bmgrp BI-VAN1MR说明书
Vanin-1 ELISA Kit (Mouse/Rat VNN1) | BI-VAN1MR
Biomedica大鼠和小鼠Vanin1 ELISA试剂盒:
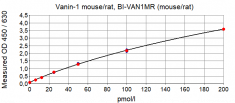
分析特征
方法
夹心ELISA,HRP / TMB,12×8孔可分离试纸
样品类型
血清,血浆和尿液
样品量
5微升/孔
测定时间
4小时/ 30分钟
灵敏度
2.31 pmol /升
标准范围
0 – 200 pmol / l(= 0 – 10.6 ng / ml)
转换系数
1 pmol / l = 52.07 pg / ml(MW:52.07 kDa)
中间运行(n = 5):≤8%CV
批量分析(n = 7):≤8%CV
特异性
内源和重组小鼠/大鼠Vanin-1。
采用
仅供研究使用。
验证数据
请参阅验证数据选项卡,以了解:精度,准确性,稀释线性,样品值
Vanin-1 ELISA试剂盒是一个4.5小时的96孔夹心ELISA,用于定量测定血清,血浆和尿液中的Vanin-1。
Vanin-1小鼠/大鼠ELISA试剂盒是一种夹心酶免疫测定法,用于定量测定小鼠或大鼠样品中的Vanin-1。该试剂盒利用重组小鼠Vanin-1作为校准物。VNN1基因在黑猩猩,恒河猴,狗,牛,小鼠,大鼠和鸡中是保守的https://www.ncbi.nlm.nih.gov/homologene/32130。
下图说明了Vanin-1夹心ELISA的原理:
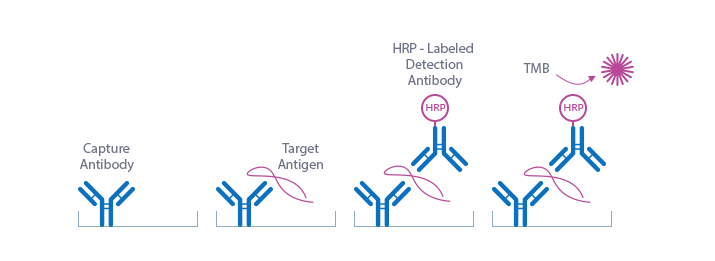
靶抗原: 小鼠/大鼠Vanin-1
靶抗原:重组小鼠Vanin-1
一步,将测定缓冲液吸移到微量滴定条的孔中。此后,将标准/对照/样品和检测抗体(多克隆绵羊抗小鼠Vanin-1-HRPO)移入孔中,并预先涂有抗小鼠Vanin-1抗体。存在于标准品/对照品/样品中的Vanin-1与孔中预包被的抗体结合,并与检测抗体形成三明治。在洗涤步骤中,将除去所有非特异性未结合的材料。在下一步中,将底物(TMB,四甲基联苯胺)移入孔中。底物的酶催化颜色变化与样品中Vanin-1的量成正比。使用标准酶标仪可以检测到这种颜色变化。吸光度的剂量响应曲线(光密度,使用从标准品获得的值,生成相对于标准品浓度的450 nm处的OD。直接从剂量响应曲线确定样品中Vanin-1的浓度。
下图显示了Mouse Vanin-1 ELISA和Rat Vanin-1 ELISA的典型标准曲线。Vanin ELISA试剂盒针对重组小鼠Vanin-1肽进行了校准:
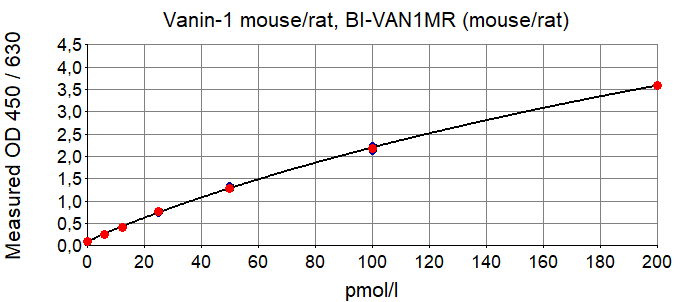
内容 | 描述 | 数量 |
盘子 | 装在带干燥剂的铝袋中的带固定器中的抗小鼠Vanin-1抗体预包被的微量滴定条 | 12 x 8测试 |
洗车场 | 洗涤浓缩液20倍 | 1 x 50毫升 |
性病 | 包含重组Mouse Vanin-1(冻干)的储备标准液(200 pmol / l) | 1个小瓶 |
CTRL键 | 对照,冻干,浓度见标签 | 1个小瓶 |
ASYBUF | 测定缓冲液,准备使用 | 1 x 7毫升 |
康杰 | 共轭多克隆绵羊抗小鼠Vanin-1抗体-HRP | 1 x 6毫升 |
潜艇 | 基材(TMB解决方案),可以立即使用 | 1 x 13毫升 |
停 | 停止解决方案,准备使用 | 1 x 7毫升 |
储存说明: Vanin-1 Mouse / Rat ELISA试剂盒中的所有试剂在4°C稳定,直到每种试剂标签上注明的有效期。
血清,血浆和尿液样本适用于此Vanin-1 ELISA分析。研究期间请勿更改样品类型。我们建议对所有样品,标准品和质控品进行重复测量。列出的所列样品收集和储存条件旨在作为一般准则。
使用EDTA,肝素或柠檬酸盐作为抗凝剂,在标准化血清分离管(SST)或标准化血液采集管中收集静脉血样。对于血清样品,让样品在室温下凝结30分钟。根据试管制造商的使用说明离心分离。立即测定采集的样品,或等分试样并保存在-25°C或更低的温度下。脂血或溶血的样品可能会产生错误的结果。样品至少要经历4次冻融循环。
无菌收集当天的一批尿(中游),直接排入无菌容器中。离心除去颗粒物,立即分析或等分并保存在-25°C或更低的温度下。样品可以经历至少四个冻融循环。
1。 | 使WASHBUF浓缩液达到室温。缓冲液浓缩物中的晶体在室温下会溶解。 |
2。 | 将WASHBUF浓缩液按1:20的比例稀释,例如50 ml WASHBUF + 950 ml蒸馏水或去离子水。进行测定时仅使用稀释的WASHBUF。 |
稀释的WASHBUF在4°C(2-8°C)下可以稳定长达一个月。
1。 | 移取200 µl蒸馏水或去离子水到储备标准液(STOCK STD)和对照(CTRL)小瓶中。准确的浓度印在每个样品瓶的标签上。 |
2。 | 在室温(18-26°C)下放置10分钟。轻轻涡旋。 |
重构的STD和CTRL在室温(18-26°C)下稳定三个小时。STD和CTRL在标签上注明的失效日期之前可稳定在-25°C或更低的温度,并且多可进行三个冻融循环。
1。 | 使用聚丙烯管,并将它们标记为STD6至STD1,如下所示(图1)。 |
2。 | 将STOCK STD标记为STD7。 |
3。 | 吸取50 µl ASYBUF(测定缓冲液)到每个标有STD6至STD1的管中。 |
4。 | 准备两倍的系列稀释液以获得STD6至STD2。用移液管吸取50 µl重新配制的STOCK STD = STD7到标有STD6的管中。*混合。继续对STD5,STD4,STD3,STD2进行系列稀释(见图1)。 |
5, | ASYBUF用作零标准品(= STD1,0 pmol / l)。 |
准备STD7至STD1
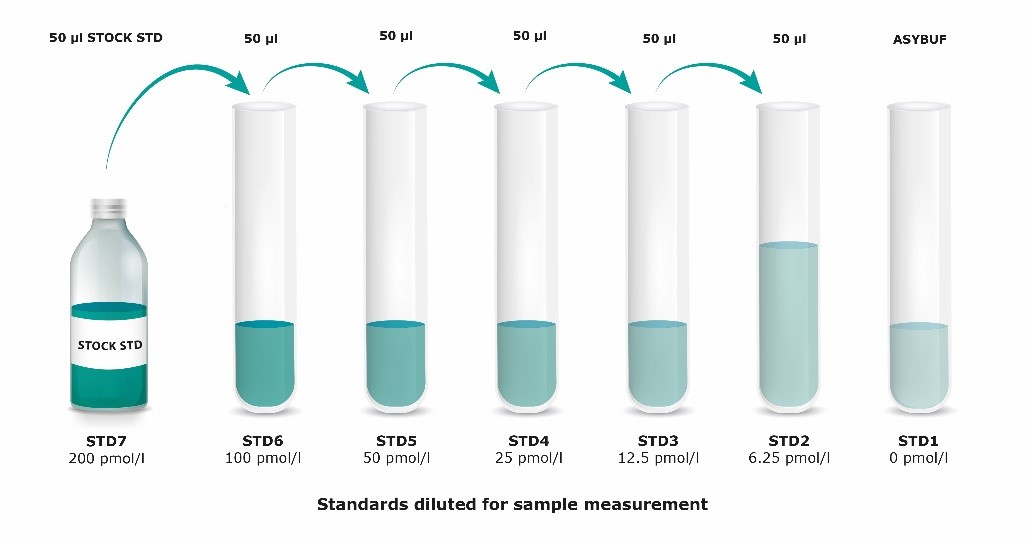
将样品置于室温并轻轻混合样品,以确保样品均匀。我们建议对所有样品进行重复测量。
值高于STD7(200 pmol / l)的样品可用ASYBUF(测定缓冲液)稀释。
鼠标样本
小鼠血清,血浆和尿液样品必须用分析缓冲液(ASYBUF)稀释1 + 7。5 µl样品+ 35 µl ASYBUF。稀释后的样品在4°C(2-8°C)下稳定过夜。因此可以在分析前一天制备稀释液。
大鼠样本
大鼠样品未经稀释即使用。
在开始测定之前,请阅读整个方案。
1。 | 使样品和试剂达到室温(18-26°C)。 |
2。 | 在协议表上标记STD / CTRL / SAMPLE(标准/对照/样品)的位置。 |
3。 | 从铝袋中取出微量滴定条。将未使用的干燥剂带在4°C的铝袋中存放。胶条在标签上标明的有效期限之前都是稳定的。 |
4。 | 移取50 µl ASYBUF(测定缓冲液,天然盖)到每个孔中。 |
5, | 将5 µl STD / CTRL / SAMPLE加到各自的孔中,一式两份。 |
6。 | 在每个孔中加入50 µl CONJ(结合物,琥珀色帽)。轻轻旋转。 |
7。 | 盖紧板,轻轻旋转并在室温(18-24°C)下孵育4小时。 |
8。 | 用300 µl稀释的WASHBUF(洗涤缓冲液)抽吸并洗孔5次。后一次洗涤后,用一块毛巾强力拍打盘子,以除去剩余的WASHBUF。 |
12 | 在每个孔中加入100 µl SUB(底物,蓝色盖)。 |
13 | 在黑暗中于室温下孵育30分钟。 |
14。 | 在每个孔中加入50 µl STOP(终止溶液,白色盖)。 |
15 | 如果可用,立即在参考630 nm的450 nm处测量吸光度。 |
使用450 nm波长(参考波长630 nm)在读板器上读取所有孔的光密度(OD)。使用能够生成四参数对数(4-PL)拟合的市售软件从标准品的吸光度读数构建标准曲线。或者,将标样在x轴上的浓度相对于每种标样在y轴上的平均吸光度作图,并通过图中的点绘制拟合曲线。除4-PL以外的曲线拟合算法尚未得到验证,用户需要对其进行评估。
从标准曲线获得样品浓度。如果需要,可通过应用转换因子将pmol / l转换为pg / ml(1 ng / ml = 18.87 pmol / l; Vanin-1小鼠/大鼠MW:53 kDa)。
计算样品的终浓度时,必须考虑各自的稀释系数。
Vanin-1是由513个氨基酸组成的GPI固定糖蛋白,由一个碱基结构域和一个酶促腈水解酶结构域组成(Boersma等,2014)。外切酶催化泛酸水解为泛酸(维生素B5)和胞嘧啶,因此参与氧化应激和炎症的调节(Maras等,1999)。Vanin-1具有广泛的组织表达,在肾小管上皮细胞中观察到高水平(Pitari等人,2000).Vanin-1的GPI锚可以通过未知的机制裂解,从而导致Vanin-1被掉进细胞外空间。
分子量 | 52.07 kDa |
细胞定位 | 细胞外质膜 |
翻译后修饰 | 糖基化,脂化(GPI锚) |
序列相似性 | Vanin蛋白家族的成员,与生物素酶家族的序列相似性 |
替代名称 | 血管非炎性分子1,Tiff66,泛酸水解酶,泛酸酶,VNN1,HDLCQ8 |
Entrez / NCBI ID | 8876 |
基因卡 | GC06M132680 |
OMIM | 603570 |
蛋白质图谱 | VNN1 |
Uniprot ID | O95497 |
Vanin-1是一种上皮细胞外酶,可激活泛素向泛酸(维生素B5)和半胱胺的转化(Pitari等,2000)。已有研究表明Vanin-1释放的半胱胺可通过抑制超氧化物歧化酶(SOD)和谷胱甘肽(GSH)等抗氧化剂的活性来促进氧化性组织损伤和炎症(Hosohata等,2011; Saghaei等,2012 )。实际上,Vanin-1基因敲除小鼠的GSH储存量较高,并且对全身伽马射线辐射引起的氧化损伤具有更高的抵抗力(Berruyer等,2004)。另一方面,一些报告表明Vanin-1也可能充当氧化应激的组织传感器。在小鼠中,可以在Vanin-1的启动子区域鉴定出类似抗氧化剂反应的元素,它们在存在氧化应激的情况下增强Vanin-1的表达(Berruyer等,2004)。同样,在人类近端肾小管细胞系中,暴露于有机溶剂后,Vanin-1的表达也被上调(Hosohata等,2011)。在大鼠肾脏缺血-再灌注后,还发现了一个涉及氧化组织损伤的模型,肾脏Vanin-1的表达也被上调(Yoshida等,2002)。
Vanin-1表达的高水平可能归因于肾小管上皮细胞,而肾小球中没有检测到表达(Hosohata等,2011; Pitari等,2000)。因此,从肾细胞释放的Vanin-1可以在尿液中检测到。在一项旨在鉴定肾小管损伤的生物标记物的研究中,Hosohata及其同事确实可以在肾毒性药物诱发的大鼠模型中证明,Vanin-1在肾小管中的表达要比其他标记物早,并掉入尿液中(Hosohata等, 2011)。随后的研究进一步证实了Vanin-1作为药物引起的急性肾损伤(Hosohata等,2012,2016a),阻塞性肾病(Washino等,2019)和肾积水(Hosohata)的早期肾小管损伤的生物标志物的有效性。等(2018),糖尿病肾病(Fugmann等,2011),高盐摄入下实验性结肠炎(Hosohata等,2014)和自发性高血压大鼠的肾脏损伤(Hosohata等,2016b; Washino等,2018)。值得注意的是,Vanin-1似乎比已建立的标志物KIM-1,NGAL或NAG具有更好的预测急性肾损伤的价值(Fugmann等,2011; Hosohata,2016; Hosohata等,2011)。
肾脏科
Vanin-1-/-小鼠表现出谷胱甘肽介导的组织对氧化应激的抗性。
Berruyer,C.,Martin,FM,Castellano,R.,Macone,A.,Malergue,F.,Garrido-Urbani,S.,Millet,V.,Imbert,J.,Duprè,S.,Pitari,G. ,Naquet,P.,Galland,F.,2004 。细胞。生物学 24,7214–7224。
 PMID:15282320; PMCID:PMC479710
PMID:15282320; PMCID:PMC479710
Vanin 1的结构:连接代谢疾病和炎症的关键酶。
Boersma,YL,Newman,J.,Adams,TE,Cowieson,N.,Krippner,G.,Bozaoglu,K.,Peat,TS,2014。ActaCrystallogr 。D生物学。Crystallogr。70,3320–3329。
 PMID:25478849
PMID:25478849
在1型糖尿病肾病大鼠模型中,vanin-1的蛋白质组学鉴定为肾脏损伤的标志物。
Fugmann,T.,Borgia,B.,Révész,C.,Godó,M.,Forsblom,C.,Hamar,P.,Holthöfer,H.,Neri,D.,Roesli,C.,2011.肾脏。80,272–281。
 PMID:21544065
PMID:21544065
肾盂尿液中的Vanin-1反映了肾积水大鼠模型的肾脏损伤。
Hosohata,K.,Jin,D.,Takai,S.,Iwanaga,K.,2018.分子科学19。
 PMID:30332759; PMCID:PMC6214032
PMID:30332759; PMCID:PMC6214032
氧化应激在药物诱发的肾损伤中的作用。
Hosohata,K.,2016年。分子科学17。
 PMID:27809280; PMCID:PMC5133827
PMID:27809280; PMCID:PMC5133827
尿vanin-1对尿路上皮癌患者顺铂诱导的肾毒性的早期预测。
Hosohata,K.,Washino,S.,Kubo,T.,Natsui,S.,Fujisaki,A.,Kurokawa,S.,Ando,H.Fujimura,A.,Morita,T.,2016a。毒理学359–360,71–75。
 PMID:27317936
PMID:27317936
高盐摄入量的自发性高血压大鼠小管损伤的早期尿液生物标志物。
Hosohata,K.,Yoshioka,D.,Tanaka,A.,Ando,H.,Fujimura,A.,2016年b。高血压。Res。39,19–26。
 PMID:26376947
PMID:26376947
实验性结肠炎大鼠中使用尿vanin-1早期发现肾脏损伤。
Hosohata,K.,Ando,H.,Fujimura,A.,2014。《应用毒理学杂志》 34,184–190 。
 PMID:23307618
PMID:23307618
尿Vanin-1作为药物诱导的急性肾损伤的早期检测的新型生物标志物。
Hosohata,K.,Ando,H.,Fujimura,A.,2012年。《药理学与实验治疗学杂志》 341,656–662。
Vanin-1:肾毒性剂引起的肾损伤的潜在生物标志物。
Hosohata,K.,Ando,H.,藤原,Y。,藤村,A.,2011。毒理学290,82–88。
 PMID:21907259
PMID:21907259
Pantetheinase是小鼠和人类vanin-1蛋白的真实身份吗?
Maras,B.,Barra,D.,Duprè,S.,Pitari,G. ,1999。FEBS来信461,149-152。
膜结合Vanin-1的Pantetheinase活性:Vanin-1缺陷小鼠组织中缺乏游离半胱胺。
Pitari,G.,Malergue,F.,Martin,F.,Philippe,JM,Massucci,MT,Chabret,C.,Maras,B.,Duprè,S.,Naquet,P.,Galland,F.,2000。FEBS信函483,149–154。
卡托普利对半胱胺诱导的十二指肠溃疡的影响。
Saghaei,F.,Karimi,I.,Jouyban,A.,Samini,M.,2012。实验。Pathol。64,373–377。
 PMID:21036019
PMID:21036019
Vanin-1,急性肾损伤的新型生物标志物,用于阻塞性肾病:一项前瞻性队列研究。
华盛顿州北区野市,细田ata市,大岛县,小河内市,小西区,中村市,佐藤市,宫川市,2019年。分子科学20。
 PMID:30791405; PMCID:PMC6412925
PMID:30791405; PMCID:PMC6412925
正常血压大鼠高盐摄入量引起的肾小管损害的早期尿液生物标志物。
Washino,S.,Hosohata,K.,Jin,D.,Takai,S.,Miyagawa,T.,2018.临床。经验 Pharmacol。生理学。45,261–268。
 PMID:29027259
PMID:29027259
监测大鼠肾脏缺血再灌注中基因表达的变化。
吉田T.,库雷拉M.,比托F.,Min H.,Ingelfinger,JR,Stears,RL,Swinford,RD,Gullans,SR,Tang,S.-S.,2002年。61,1646–1654.。
 PMID:11967014
PMID:11967014

